вт, 02 Июл 2013 22:40
Миронов В.М., Самко А.Н., Меркулов Е.В.
Имплантация биорастворимого сосудистого стента Absorb.
ФГБУ «РКНПК» МЗ РФ, Москва.
Введение
В 1977 году Andreas Gruntzig произвел революцию в лечении пациентов с ишемической болезнью сердца, впервые выполнив транслюминальную баллонную ангиопластику. Он доказал, что гемодинамически значимые сужения коронарных артерий можно устранить с помощью баллонной дилатации, которая приводит к расширению сосуда и восстановлению кровотока, и как следствие к уменьшению ишемии миокарда и симптомов стенокардии с ней связанной. Хотя на тот момент этот метод был большим прорывом в кардиологии, он имел ряд отрицательных сторон. В первые часы после дилатации частым осложнением были острые окклюзии, вызванные сочетанием диссекции интимы при раздувании баллона и эластического спадения сосуда, которые требовали экстренных вмешательств, в более отдаленные сроки частым осложнением были рестенозы, как следствие разрастания неоинтимы в ответ на баротравму сосуда (1).
Некоторые из недостатков баллонной ангиопластики удалось устранить с появлением голометалических стентов (ГМС). Стало возможным прижатие балками металлического стента травмированной интимы артерии, и тем самым снизить число тромбозов и спадений артерии (рекойл) как в госпитальном, так и отдаленном периоде. Но, несмотря на преимущества нового метода и обнадеживающие результаты первых исследований, в дальнейшем стало очевидным, что ГМС не спасают от гиперплазии неоинтимы, проявляющейся рестенозами внутри стентов и встречавшейся по данным различных исследований в 16-44% случаев (2).
Большое количество рестенозов при установке ГМС послужило толчком к появлению стентов с лекарственным покрытием (СЛП). Они стали следующим шагом в эволюции рентгеноэндоваскулярного лечения коронарного атеросклероза. Первые исследования показывали впечатляющие результаты, в некоторых подгруппах пациентов удалось достигнуть 0% рестеноза, хотя при исследовании больших групп пациентов с различной выраженностью атеросклеротического поражения и сопутствующих заболеваний рестеноз достигал 7- 16% (3-5). В последствии стали накапливаться данные об осложнениях связанных с установкой стентов с лекарственным покрытием. У первого поколения лекарственных стентов нечастыми осложнениями были подострые и поздние тромбозы, как следствие замедленного заживления травмы, вызванной балками стента и позднее покрытие структур стента эндотелием, затем было показано, что неполное прилегание (мальапозиция) стента к стенке сосуда, особенно в месте богатой липидами атеросклеротической бляшки, также может приводить к тромбозу стента (6-8).
Перспектива использования временного сосудистого стента, или биорастворимого каркаса, всегда была целью интервенционного сообщества. Такое устройство должно обладать радиальной жесткостью, чтобы противостоять острому спадению сосуда после завершения вмешательства, а также полностью рассасываться в отдаленном периоде, что приводило бы к восстановлению биологических и физиологических свойств сосуда. В настоящее время широко обсуждаются потенциальные преимущества этой новой технологии, которая получила название "сосудистой репаративной терапии», по сравнению с применением обычных металлических стентов и металлических стентов с лекарственным покрытием.
Структура биорастворимого сосудистого каркаса (БСК).
БСК Absorb имеет платформу, изготовленную из поли-L-лактида (PLLA), который успешно используется во многих областях медицины (рассасывающиеся швы, ортопедические импланты, наполнитель аппарата для гемодиализа). Поли-L-лактид является полукристаллическим полимером, состоящим из тонких пластинок кристаллов взаимосвязанных случайными цепями полимера, образующего аморфный сегмент. Платформа по своей форме напоминает рисунок стента Multi-Link, покрыта смесью 1:1 рассасывающегося полимера поли-D,L-лактида и антипролиферативного препарата Эверолимус (8,2 мкг/мм). На проксимальном и дистальном концах находятся пары рентгеноконтрастных маркеров из платины, позволяющие визуализировать место имплантации БСК при коронарной ангиографии. БСК закреплен на системе доставки, имеющей те же характеристики, что и система доставки металлических стентов последнего поколения того же производителя (Рис. 1).

Рисунок 1. Биорастворимый сосудистый каркас Absorb с парой рентгеноконтрастных платиновых маркеров.
Сосудистая репаративная терапия (СРТ):
СРТ основана на предположении, что поддержка сосуда изнутри и доставка лекарственного вещества в пораженный атеросклерозом участок коронарной артерии необходимы непродолжительное время после эндоваскулярного вмешательства. Несколько исследований поддержали эту концепцию и доказали отсутствие клинической пользы от долгосрочного постоянного нахождения стента в сосуде (2,10-14). Использование биорастворимого сосудистого каркаса (БСК) Absorb исключает постоянное нахождение инородного тела в организме и предполагает возвращение сосуду его физиологических функций.
В отличие от стентирования, которое предполагает только одно действие –реваскуляризацию, установка биорастворимого каркаса предполагает три фазы процесса: реваскуляризацию, восстановление и растворение. Все эти три фазы являются составными частыми СРТ.
Реваскуляризация.
Фаза реваскуляризации длится около 3 месяцев после вмешательства (Рис 2), в течение которых БСК показал схожие клинические результаты по сравнению со стентами с лекарственным покрытием. По таким показателям как хорошая доставляемость, минимальное спадение (рекойл) в остром периоде, высокая радиальная сила и контролированное высвобождение антипролиферативного препарата Эверолимус (для минимизации роста неоинтимы) БСК и стенты с лекарственным покрытием последнего поколения достоверно не различались.
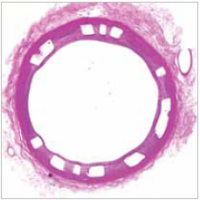
Рисунок 2: Фаза реваскуляризации, 3 месяца после имплантации. Балки БСК покрыты слоем эндотелия.
Восстановление.
В фазу восстановления БСК постепенно прекращает выполнять поддерживающую функцию, растворяясь, превращается из цельного каркаса в разрозненную структуру, внедренную в новообразованную эндотелиальную ткань (Рис. 3). В конце фазы восстановления БСК перестает механически сдерживать сосуд, что позволяет артерии вернуться в свое нормальное состояние, нескованное металлическим каркасом.
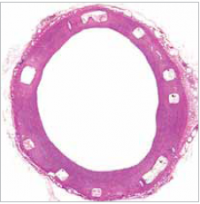
Рисунок 3. Фаза восстановления, 6 месяцев после имплантации. БСК постепенно прекращает выполнять поддерживающую функцию, растворяясь, превращается из цельного каркаса в разрозненную структуру, внедренную в новообразованную эндотелиальную ткань.
Растворение.
Фаза растворения начинается, когда каркас перестал выполнять свою поддерживающую функцию, в отсутствии сдерживающих структур артерия восстанавливает способность к реагированию на физиологические стимулы (Рис. 4). БСК в этот период представляет собой инертные вкрапления в сосудистой стенке, которые в период 12-24 месяца после установки постепенно распадаются на молочную кислоту, которая, в конечном счете, превращается в диоксид углерода и воду. Молочная кислота легко превращается в лактат в норме присутствующий в кровотоке и участвующий в метаболических процессах человеческого организма. Уровень лактата в крови во время растворения БСК не выходит за рамки нормальных значений, как в покое, так и при физической нагрузке. Через 2 года, на месте балок БСК находятся скопления протеогликанов, отсутствуют признаки воспаления. Через 3 года начинается замещение бывших балок БСК фибробластами, гладкомышечными клетками и межклеточным матриксом (Рис. 5). Через 4 года места, в которых находились балки, в значительной степени неразличимы, так как соединительная ткань выполнила их место и стала неотъемлемой частью артериальной стенки (15). Это доброкачественное образование неоинтимы и замена БСК соединительной тканью, давшее представление о возможном механизме регрессии бляшек, было продемонстрировано в исследовании ABSORB (16). Учитывая то, что соединительная ткань со временем естественно сжимается, БСК провоцирует образование фиброзной покрышки над атеросклеротической бляшкой, которая со временем уменьшается в размерах и стабилизируется.
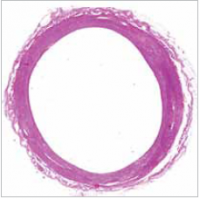
Рисунок 4: Фаза растворения. БСК в этот период представляет собой инертные вкрапления в сосудистой стенке, которые в период 12-24 месяца после установки постепенно распадаются на молочную кислоту, которая, в конечном счете, превращается в диоксид углерода и воду.

Рисунок 5: Через 3 года начинается замещение бывших балок БСК фибробластами, гладкомышечными клетками и межклеточным матриксом.
Наш опыт установки БСК Absorb.
В августе и декабре 2012 впервые в России в РКНПК МЗ РФ были установлены 3 (три) БСК Absorb 2-м пациентам с ИБС и стенозами в коронарных артериях. Ниже приведем клинический пример.
Пациентка Н. 61 года поступила в РКНПК МЗ РФ с клиникой стенокардии III-IV ФК, сохраняющейся на фоне многокомпонентной антиангинальной терапии в условиях ограничения физической активности. При МСКТ коронарных артерий определялись кальцинаты в проекции стенок коронарных артерий: в среднем сегменте ПНА объемом 25 мм³, КИ – 28 ЕД, в проксимальном сегменте ОА объемом 12 мм³, КИ 12 ЕД, во всех сегментах ПКА 21 мм³, КИ -24 ЕД. Суммарный КИ = 64 ЕД. При коронарной ангиографии от 5.12.12 года: сбалансированный тип коронарного кровоснабжения. Ствол левой коронарной артерии не изменен. Передняя нисходящая артерия (ПНА) в проксимальном сегменте с переходом на средний сегмент стенозирована на 71-91% (рис. 6) при компьютерном анализе (QCA), далее имеет гемодинамически незначимые неровности контуров. Огибающая артерия (ОА) имеет неровности контуров в среднем сегменте, артерия тупого края не изменена. Правая коронарная артерия с неровными контурами на всем протяжении, без гемодинамически значимого стенозирования. Во время коронарной ангиографии было проведено измерение фракционного резерва кровотока (ФРК) в ПНА и ОА. ФРК в среднем сегменте ПНА = 0.64, в дистальном сегменте ОА = 0,97. Под местной анестезией раствором лидокаина 2%-10 мл правым радиальным доступом был установлен интродюсер 6F. К устью левой коронарной артерии подведен направляющий катетер PB 3,5 и в дистальный сегмент ПНА проведен интракоронарный проводник. После ряда предилатаций баллонными катетерами 3,0х20 и 3,5х20 мм, было выполнено внутрисосудистое ультразвуковое исследование (ВСУЗИ): в проксимальном и среднем сегменте ПНА определяется гетерогенная эксцентрическая атеросклеротическая бляшка с признаками кальциноза, сужающая просвет на 72,1% площади (рис.7) , протяженностью 37 мм, должный диаметр ПНА в проксимальном и среднем сегменте 3,7 мм. В проксимальном и среднем сегменте ПНА последовательно установлены два биорастворимых сосудистых каркасов Absorb 3,5х28 и 3,5х12мм, давлением до 14 атмосфер, длительностью до 30 сек. Выполнена постдилатация БСК баллонным катетером 3,5х20мм, давлением до 18 атм, длительностью до 30 сек (Рис.8). При контрольном ВСУЗИ в проксимальном и среднем сегменте ПНА определяются БСК полностью расправленные, без признаков пристеночного тромбоза и краевых диссекций. Диаметр просвет артерии в месте установки БСК 3,7 мм (Рис.9). Проводник, катетер и интродюсер удалены выполнен гемостаз места пункции, наложена тугая асептическая повязка. После вмешательства приступы стенокардии не рецидивировали, через 2 дня пациентка была выписана домой в удовлетворительном состоянии.
Заключение.
Наш первый опыт имплантации биорастворимых каркасов показал их эффективность. К особенностям установки БСК можно отнести то, что в отличие от обычных металлических стентов для установки которых требуется минимальная подготовка сосуда перед имплантацией, при установке биорастворимых каркасов требуется максимальная подготовка стеноза перед имплантацией с помощью баллонирования. Биорастворимые технологии предполагают восстановление сосуда до более естественного состояния, сохраняя его исходные физиологические функции. В сосуде отсутствует источник хронического раздражения и воспаления, а, следовательно, нет необходимости в длительной двойной антиагрегантной терапии. К тому же, сосуд остается свободным для дальнейшего (при необходимости) лечения как эндоваскулярного, так и хирургического (АКШ-МКШ). Наличие рентгеноконтрастных меток на концах каркаса дает возможность использовать неинвазивные методы визуализации в случае необходимости. При динамическом дальнейшем наблюдении МСКТ с контрастированием дает возможность оценить состояние каркаса и его проходимости в отличие от ГМС и СЛП. В настоящее время биорастворимые технологии всё ещё находятся в начальном состоянии своего развития, но они быстро прогрессируют и, возможно, в скором времени, потеснят обычные металлические стенты из шкафов рентгеноперационных кабинетов (и коронарных артерий пациентов). Но пока для более полной оценки эффективности и безопасности биорастворимых сосудистых каркасов – стентов, устанавливающихся в стенозах коронарных артерий, требуются большие рандомизированные исследования и длительный период наблюдения за отдаленными (3-5 лет) результатами лечения.
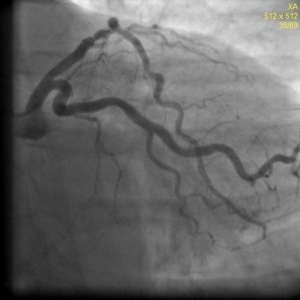
Рисунок 6. Левая коронарная артерия. Стеноз проксимального и среднего сегмента передней нисходящей артерии.

Рисунок 7. ВСУЗИ ПНА до установки БСК Absorb. Гетерогенная эксцентрическая атеросклеротическая бляшка с признаками кальциноза.
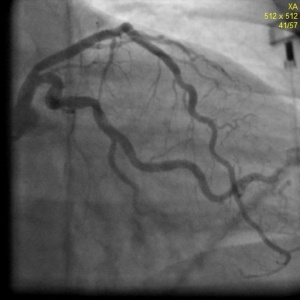
Рисунок 8: Результат ангиопластики и установки БСК Absorb.
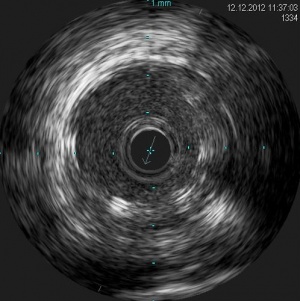
Рисунок 9. ВСУЗИ после установки БСК Absorb. Видны балки БСК.
Список литературы:
1. Grüntzig A. Transluminal dilatation of coronary artery stenosis. Lancet. 1978; 1: 263.
2. Serruys PW, de Jaegere P, Kiemeneij F, et al. A comparison of balloon-expandable-stent implantation with balloon angioplasty in patients with coronary artery disease. Benestent Study Group. N Engl J Med. 1994; 331: 489-495
3. Morice MC, Serruys PW, Sousa JE, et al. A randomized comparison of a sirolimus-eluting stent with a standard stent for coronary revascularization. N Engl J Med. 2002; 346: 1773-1780.
4. Самко А.Н. Стенты с лекарственным покрытием при лечении острого инфаркта миокарда (современное состояние вопроса). В кн.: Сердечно-сосудистая патология. Сборник трудов к 80-летию Е.И.Чазова. М.: Медиа Медика., 2009, с. 258-265.
5. Garg S, Serruys PW. Coronary stents: looking forward. J Am Coll Cardiol. 2010; 56: S43-78.
6. Byrne RA, Eberle S, Kastrati A, et al. Distribution of angiographic measures of restenosis after drug-eluting stent implantation. Heart. 2009; 95: 1572-1578.
7. Sousa JE, Costa MA, Abizaid A, et al. Lack of neointimal proliferation after implantation of sirolimus-coated stents in human coronary arteries: a quantitative coronary angiography and three-dimensional intravascular ultrasound study. Circulation. 2001; 103: 192-195.
8. Räber L, Wohlwend L, Wigger M, et al. Five-year clinical and angiographic outcomes of a randomized comparison of sirolimus-eluting and paclitaxel-eluting stents: results of the Sirolimus-Eluting Versus Paclitaxel-Eluting Stents for Coronary Revascularization LATE trial. Circulation. 2011; 123: 2819-2828.
9. Serruys PW, Luijten HE, Beatt KJ, Geuskens R, De Feyter PJ, van den Brand M, Reiber JH, ten Katen HJ, van Es GA Hugenholtz PG. Incidence of restenosis after successful coronary angioplasty, a time-related phenomenon. A quantitative angiographic study in 342 consecutive patients at 1, 2. 3, and 4 months. Circulation 1988 Feb;77(2):361-71.
10. Nobuyoshi M, Kimura T, Nosaka H, Mioka S, Ueno K, Yokoi H, Hamasaki N, Horiuchi H, Ohishi H. Restenosis after successful percutaneous transluminal coronary angioplasty: serial angiographic follow-up of 229 patients. J Am Coll Cardiol. 1988 Sep; 12(3):616-23.
11. Asakura M, Ueda Y, Nanto S, Hirayama A, Adachi T, Kitakaze M, Hori M, Kodama K. Remodeling of in-stent neointima, which became thinner and transparent over 3 years: serial angiographic and angioscopic follow-up. Circulation. 1998 May;97(20):2003-6.
12. Witkowski A, Ruzyłło W, Gil R, Górecka B, Purzycki Z, Kośmider M, Poloński L, Lekston A, Gasior M, Zmudka K, Pieniazek P, Buszman P, Drzewiecki J, Ciećwierz D, Sadowski Z. A randomized comparison of elective high-pressure stenting with balloon angioplasty: six-month angiographic and two-year clinical follow-up. On behalf of AS (Angioplasty or Stent) trial investigators. Am Heart J. 2000 Aug;140(2):264-71.
13. Betriu A, Masotti M, Serra A, Alonso J, Fernández-Avilés F, Gimeno F, Colman T, Zueco J, Delcan JL, García E, Calabuig J.Randomized comparison of coronary stent implantation and balloon angioplasty in the treatment of de novo coronary artery lesions (START): a four-year follow-up.J Am CollCardiol. 1999 Nov 1;34(5):1498-506.
14. Kandzari DE, Tuttle RH, Zidar JP, Jollis JG.Comparison of long-term (seven year) outcomes among patients undergoing percutaneous coronary revascularization with versus without stenting. Am J Cardiol. 2006 May 15;97(10):1467-72.
15. Onuma Y, Serruys PW, Perkins LE, et al: Intracoronary optical coherence tomography and histology at 1 month and 2, 3, and 4 years after implantation of everolimus-eluting bioresorbable vascular scaffolds in a porcine coronary artery model: an attempt to decipher the human optical coherence tomography images in the ABSORB trial. Circulation. 2010; 122: 2288-2300.
16. Ormiston JA, Serruys PW, Regar E, et al. A bioabsorbable everolimus-eluting coronary stent system for patients with single de-novo coronary artery lesions (ABSORB): a prospective open-label trial. Lancet. 2008; 371: 899-907.